Esperança contra doença rara
Em teste com 126 participantes, tratamento aplicado na coluna aprimorou de modo significativo a capacidade de realizar movimentos
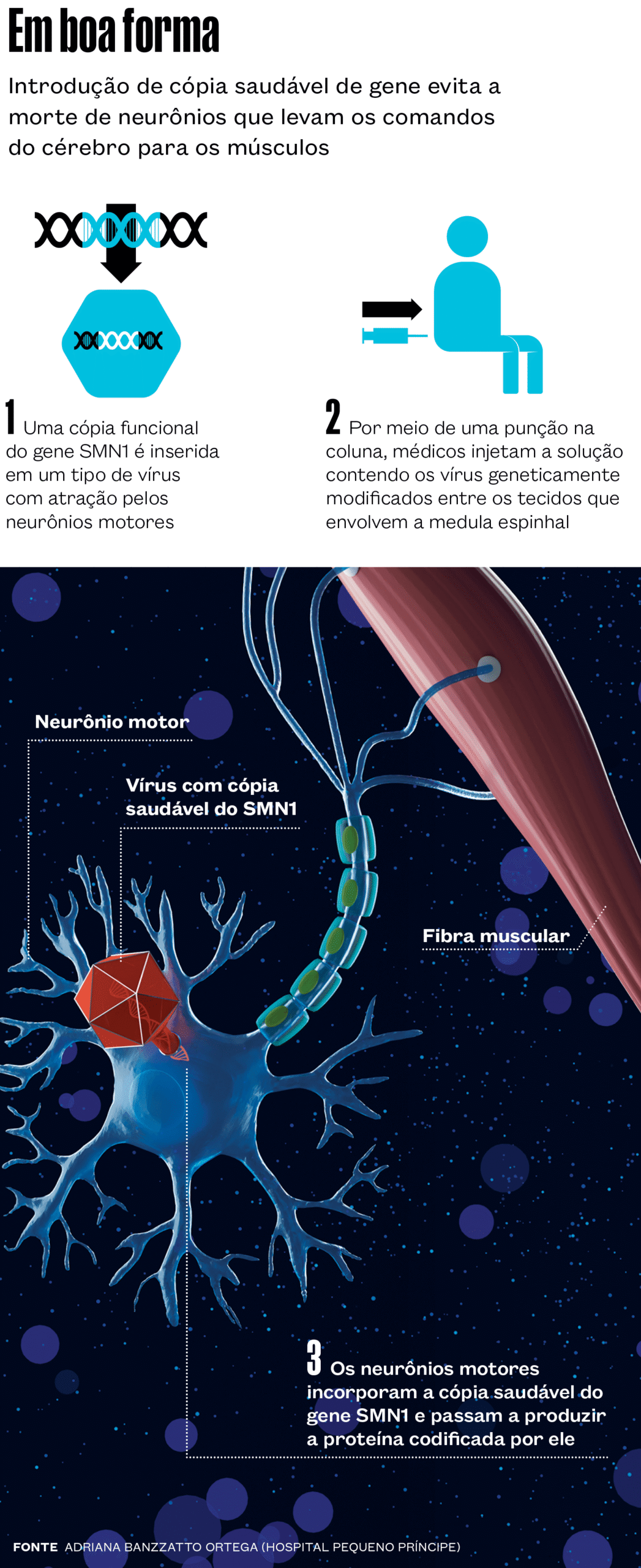
Um tratamento em dose única aplicado na região lombar da coluna vertebral mostrou resultados promissores para tratar uma doença rara – a atrofia muscular espinhal (AME) – em crianças com mais de 2 anos e adolescentes. Uma versão anterior da terapia, administrada na corrente sanguínea, era indicada para menores de 2 anos. Na nova abordagem, o material que corrige o defeito genético causador da AME foi injetado entre as membranas que protegem a medula espinhal (administração intratecal), facilitando a sua chegada ao alvo.
A AME é uma doença genética irreversível, causada por um defeito que leva à perda de função das duas cópias (materna e paterna) do gene SMN1. Esse gene codifica uma proteína – a survival motor neuron, SMN – que promove a sobrevivência do neurônio motor. Sem ela, os neurônios motores da medula espinhal morrem e deixam de transmitir para os músculos os comandos do cérebro. Como consequência, ocorre uma perda progressiva do tônus e da força muscular, e a criança apresenta problemas para manter o corpo ereto, sentar-se, segurar objetos, engolir e até mesmo respirar. Nos casos extremos, a AME leva à morte precoce, ainda na infância.
No novo tratamento proposto, um vírus modificado em laboratório para se tornar inofensivo transporta para as células da medula espinhal uma cópia saudável do SMN1. Em um teste com 126 participantes de 14 países, entre eles o Brasil, essa terapia gênica melhorou de modo significativo a capacidade de crianças e adolescentes de manter a postura do corpo e realizar alguns movimentos. Os resultados foram apresentados em um artigo publicado em dezembro na revista Nature Medicine.
Atualmente, há três tratamentos aprovados para AME. Todos tentam aumentar a disponibilidade da proteína SMN e estão entre as terapias mais caras do mundo. Dois deles são compostos que aprimoram o funcionamento do SMN2, uma espécie de gene reserva produtor de uma proteína similar à SMN1. São o nusinersen, comercializado pelo laboratório norte-americano Biogen com o nome de Spinraza, e o risdiplam, vendido pela farmacêutica suíça Roche como Evrysdi. O primeiro é de administração intratecal, feita por meio de punções lombares periódicas, a um custo unitário de cerca de R$ 680 mil – após o primeiro ano de tratamento, o gasto anual fica na casa dos R$ 2 milhões. O segundo é feito por via oral e sai por R$ 1,3 milhão por ano. Ambos são terapias que precisam ser mantidas ao longo da vida para preservar os efeitos benéficos.
A terceira opção é a terapia gênica que agora foi testada em sua versão intratecal. Ela tem o nome técnico complicado de onasemnogene abeparvovec e é comercializada como Zolgensma pela empresa farmacêutica suíça Novartis. Usado em dose única, tem um custo estimado em quase R$ 7 milhões. Antes administrada via endovenosa a bebês e crianças de no máximo 21 quilos, ela usa um vírus geneticamente modificado – o AAV9 – para levar uma cópia funcional do gene SMN1 ao organismo. No ensaio clínico atual, os pesquisadores fizeram a aplicação intratecal do onasemnogene abeparvovec, o que permite ao vírus transportando a forma saudável do SMN1 chegar mais facilmente à medula espinhal, onde estão os neurônios motores – essa abordagem reduz a exposição de outros tecidos ao vírus.
No Brasil, há cerca de 1,8 mil pessoas com AME, segundo o cadastro do Instituto Nacional de Atrofia Muscular Espinhal (Iname), e os três tratamentos são oferecidos pelo Sistema Único de Saúde (SUS). Por causa do custo elevado, tanto aqui quanto no exterior pesquisadores e formuladores de políticas públicas de saúde buscam identificar, entre as alternativas disponíveis, o tratamento que apresente a melhor relação entre custo e benefício.
No trabalho publicado na Nature Medicine, a equipe liderada pelo neuropediatra Richard Finkel, do Hospital de Pesquisa Infantil Saint Jude, no Tennessee, Estados Unidos, avaliou a segurança e o desempenho da terapia gênica intratecal em crianças e adolescentes com idade entre 2 e 17 anos e 11 meses atendidas em 29 centros de 14 países. No Brasil, participaram equipes do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo (FM-USP), na capital paulista, do Hospital Erastinho, em Curitiba, no Paraná, do Hospital de Clínicas de Porto Alegre, no Rio Grande do Sul, e do Hospital de Clínicas da Universidade Estadual de Campinas (Unicamp), no interior de São Paulo.
Os 126 integrantes do estudo tinham AME e nunca haviam recebido tratamento. Eles começaram a apresentar os sintomas da doença menos de seis meses antes da inclusão no estudo e eram capazes de se sentar, mas não de caminhar de modo independente. Dos participantes, 75 receberam a aplicação do medicamento por meio de uma punção lombar. Os outros 51 integraram o grupo de controle. Nestes, os pesquisadores realizaram uma perfuração mais superficial, sem a injeção de líquido. Todos estavam sob efeito de anestesia durante o procedimento.
Tratamento estabilizou a doença e aumentou a autonomia para se movimentar
“Como o número de neurônios motores é definido desde o nascimento [cada indivíduo nasce com um certo número dessas células, que não se multiplicam nem são repostas ao longo da vida], a dose do tratamento por via intratecal é fixa”, conta a neurologista Adriana Banzzatto Ortega, do Hospital Pequeno Príncipe, uma das autoras do estudo. “Na versão endovenosa do Zolgensma, a dosagem varia de acordo com o peso porque o tratamento é transportado pelo sangue e se distribui por todo o corpo”, explica.
Depois de administrada a terapia gênica ou o procedimento placebo, os pesquisadores acompanharam a evolução dos participantes por um ano. O desempenho dos dois grupos foi medido por uma escala que avalia habilidades motoras, como o controle do tronco, a capacidade de se sentar e de realizar movimentos voluntários. No primeiro mês após o procedimento, as crianças e adolescentes tratadas com a terapia gênica intratecal apresentaram uma melhora modesta, mas significativa dos pontos de vista estatístico e clínico. Em média, o escore deles foi 2,4 pontos mais elevado do que antes do tratamento. Esse efeito durou todo o período de acompanhamento. Já no grupo de controle, a melhora foi de 0,5 ponto. Esses valores são medidos em uma escala que vai de zero a 66 pontos, sendo zero o indicador de incapacidade de realizar atividades de modo independente, e 66 o de alta habilidade motora, como andar sem ajuda de outras pessoas. Se aprovado pela Agência Nacional de Vigilância Sanitária (Anvisa), o tratamento intratecal terá seu custo determinado mais adiante no país.
“Sem tratamento, os pacientes costumam apresentar uma redução média anual de cerca de 2 pontos na escala de mobilidade usada no estudo”, conta Ortega. “Com a terapia, além de estabilização, houve o ganho de 1 a 2 pontos. Isso tem impacto na autonomia dessas crianças e adolescentes, permitindo realizar atividades como se transferir da cadeira de rodas para a cama”, completa.
Com relação à segurança, o perfil de efeitos adversos foi semelhante nos dois grupos. Os eventos mais frequentes foram infecções respiratórias leves, febre e vômito. “A observação de poucos efeitos adversos após um ano é um sinal positivo, mas são necessários estudos de acompanhamento mais robustos para confirmar se a nova via de administração pode se revelar uma alternativa mais eficaz do que as terapias já disponíveis”, afirma a neurologista Alzira Siqueira de Carvalho, da Faculdade de Medicina do ABC (FMABC), que não fez parte do estudo. Ela coordena o Ambulatório de Doenças Neuromusculares da FMABC e participou de pesquisas no exterior mostrando que a identificação precoce da AME e o início rápido do tratamento são fundamentais para melhorar a evolução da criança. “Tratar antes do aparecimento dos sintomas é o que realmente impede a progressão da doença”, explica.
Matéria: Mariana Ceci | Jornal da Unesp